

摘 要目的:探讨完全达芬奇机器人手工缝合消化道重建技术在全胃切除术中应用的可行性和安全性。方法:回顾性分析2015年7月~2018年6月东部战区总医院胃癌患者行全胃根治性切除术的临床资料。根据手术方式分为完全机器人全胃切除(Robot-assistedtotalgastrectomy,RATG)组、腹腔镜辅助全胃切除(Laparoscopicassistedtotalgastrectomy,LATG)组。RATG组行机器人镜下腔内手工缝合消化道重建,采用UncutRoux-en-Y重建方案;LATG组行体外吻合器消化道重建,采用传统Roux-en-Y重建方案。观察分析两组患者手术指标、术后康复指标、标本肿瘤学指标、经济学指标及术后并发症情况。结果:两组100例患者均顺利完成手术。RATG组较LATG组腹部切口短[(3.95±0.64)cmVs(10.38±1.79)cm,P<0.001],术中出血量少[(57.10±20.55)mlVs(98.20±28.44)ml,P<0.001],但手术时间长[(201.66±16.59)minVs(156.14±16.69)min,P<0.001],消化道重建耗时长[(56.70±8.78)minVs(36.60±8.17)min,P<0.001],住院费用高[(8.55±1.78)万元Vs(6.39±0.86)万元,P<0.001]。RATG组较LATG组术后住院时间短[(5.84±4.76)dVs(6.98±4.31)d,P=0.213],但差异无统计学意义。两组患者在术后视觉疼痛评分(VAS)、术后TNM分期、淋巴结清扫数目、阳性淋巴数目、术后首次排气时间、首次下床活动时间、首次进食流质时间及术后并发症方面的差异均无统计学意义(P>0.05)。结论:完全达芬奇机器人手工缝合消化道重建技术在全胃切除术中的应用是安全、可行的。
关键词 机器人手术系统;腹腔镜;胃癌;胃切除术
据2018年全球癌症数据统计,胃癌发病率居全球恶性肿瘤第5位,其死亡率居第3位[1]。我国是胃癌大国,数据显示我国每年新发病例约48万,占全球发病率的40%[2]。目前总体治疗策略仍然是以外科干预为主的综合治疗。自1994年Kitano报道首例腹腔镜胃癌手术后,经过二十多年的摸索创新,腹腔镜胃癌根治术已经获得认可和推广[3],自此胃癌手术进入微创时代。但受制于本身的局限性,腹腔镜在消化道重建方面的应用仍存在困难和争议。腹腔镜胃癌根治术通常需要通过腹部辅助切口在体外完成消化道重建,然而腹部辅助切口并不小,无法很好地体现微创的优势。另外完全腔镜下的消化道重建难度大,对吻合器械依赖度高、对术者要求高,而且学习曲线长。达芬奇机器人手术系统的发明和应用一定程度上克服了腹腔镜的局限性,利用其7个自由度的仿真手腕和三维放大的高清手术视野等优势实现了机器人镜下手工缝合消化道重建,摆脱了对吻合器械的依赖,实现了真正意义上的微创手术。本临床治疗中心开展达芬奇机器人胃肠手术较早,积累了一千余例的手术经验,本研究对完全机器人全胃切除术后镜下手工消化道重建方法进行分享。
1 资料与方法
1.1临床资料
回顾性分析2015年7月~2018年6月在东部战区总医院行全胃根治性切除术胃癌患者的临床资料,选取50例行完全达芬奇机器人镜下手工缝合消化道重建全胃切除术的患者为试验组(RATG组),并随机选取同期50例行腹腔镜辅助全胃切除术的胃癌患者作为对照(LATG组)。所有患者均已完善术前检查明确病情及术前风险评估,排除手术禁忌证,并自愿选择接受机器人或腹腔镜手术,签署手术知情同意书。两组患者一般资料的差异均无统计学意义(P>0.05,见表1)。病例纳入标准:①术前经胃镜检查及病理诊断明确;②术前CT评估肿瘤分期为Ⅰ、Ⅱ、Ⅲ期;③行全胃切除的患者;④术前美国麻醉医师协会(ASA)分级为Ⅰ级或Ⅱ级,无明确手术禁忌证。病例排除标准:①严重心血管或呼吸系统疾病,肝或肾功能衰竭;②姑息切除手术;③联合脏器切除;④既往有胃部分切除手术史;⑤远处器官转移。
1.2方法
1.2.1 围手术期管理
围手术期管理遵循加速康复外科治疗方案[4]。加速康复外科处理措施有二十余条,重点执行的关键措施包括:①术前不常规禁食,予以口服碳水化合物;②不常规行肠道准备;③精准液体治疗;④多模式镇痛;⑤早期经口进食;⑥早期下床活动;⑦优化导管管理(不常规放置鼻胃管,尽早去除腹腔引流管及导尿管)。该方案由加速康复外科专科护士全程参与,宣教加速康复外科围手术期知识、指导饮食与活动,记录相关康复指标。
1.2.2 机器人组手术
1.2.2.1 患者及机器人手术系统布局:全身麻醉后,患者取头高脚低仰卧位(20°),机器人器械臂车置于患者头侧,视频推车放在患者的右侧,台上助手站在患者的左侧。主刀医生坐于离手术台约3m外的机器人控制台。
1.2.2.2 腹部Trocar布局:采用五孔法(如图1A),于脐下取长约1cm皮肤切口,置入气腹针,建立气腹,气腹压控制在12~15mmHg,并置入12mmTrocar作为机器人镜头孔。于左侧锁骨中线平脐处置入12mmTrocar作为助手操作辅助孔。分别于左侧锁骨中线平脐、左侧腋前线肋下2cm、右侧腋前线肋下2cm置入3枚8mmTrocar作为机器人操作器械孔。
1.2.2.3 淋巴结清扫:根据第5版日本《胃癌治疗指南》[5]实行D2淋巴结清扫。清扫顺序遵循江志伟教授提出的“斯洛克”路径。打开小网膜至肝缘,锁扣夹将荷包线固定于肝缘的韧带,体外牵拉固定悬吊肝脏,暴露术野。将大网膜掀至上腹部,超声刀沿横结肠上缘向脾曲切除大网膜,于结肠脾曲游离胃网膜左血管并离断,完成第4sb组淋巴结清扫。再沿结肠上缘向右切除大网膜,游离胃网膜右血管并离断,完成第4d组淋巴结清扫,继续向十二指肠方向清扫,完成幽门下第6组淋巴结清扫。于胃窦小弯侧向十二指肠游离,裸化并离断胃右血管,完成幽门上第5组淋巴结清扫。镜下直线切割闭合器离断十二指肠。超声刀裸化胃左动脉、肝总动脉、腹腔动脉、肝动脉,并离断胃左动脉,完成第7、8a、9、12a组淋巴结清扫。打开胰腺上缘背膜,裸化脾动脉及脾门血管,离断胃后动脉,完成第11组淋巴结清扫。超声刀沿右侧膈肌脚向贲门右侧游离,完成第1、3组淋巴结清扫。沿胃底向贲门左侧游离,断胃短血管,完成第4sa组淋巴结清扫,继续向食管左侧清扫,完成第2组淋巴结清扫。镜下直线切割闭合器离断食道。标本置入标本袋中并暂时置于盆腔。
1.2.2.4 消化道重建(UncutRoux-Y吻合):①食道空肠吻合(端侧吻合):选用两根3-0单针自固定免打结缝线(倒刺线),长度为30cm,并采用双针四步连续缝合法完成食道空肠吻合。行食道空肠吻合前,为避免食道回缩,用3-0可吸收缝线将食道左右两侧固定于膈肌角,尽量使暴露在腹腔的食道残端长度在1cm以上,以利于吻合。提起距Treitz韧带30~40cm处空肠,将其移近食道残端,用第1根倒刺线自右往左浆肌层连续缝合固定食道后壁与空肠对系膜肠壁。缝针间距控制在0.3~0.5cm,缝合固定长度与食道径相当即可,超声刀平行于食道空肠缝线打开食道后壁,且超声刀平行于食道空肠缝线打开空肠对系膜缘肠壁。用第2根倒刺线自右向左全层连续缝合食道后壁切缘与空肠后切缘,完成食道空肠切口后壁吻合。进针方向为内进内出(食道内侧进针、空肠内侧出针)。缝合过程中,3号臂可牵拉食道残端暴露食道后壁切缘。超声刀切除食道残端吻合钉,第2根倒刺线继续自左向右全层连续缝合食道前切缘与空肠前切缘。缝合食道空肠吻合口时缝针方向要调整为外进外出(食道外侧进针、空肠外侧出针)。用第1根倒刺线自左向右浆肌层连续缝合包埋吻合口前壁,并连续包埋吻合后壁,完成食道空肠吻合口1.5圈的包埋。双股4号线于食道空肠吻合口下3cm结扎输入袢,确保食物经输出袢进入远端空肠。②空肠-空肠吻合(侧侧吻合):选用两根3-0单针倒刺线,长度为30cm,并采用双针四步连续缝合法完成食道空肠吻合。选取距Treitz韧带15cm处输入袢的空肠与距食道空肠吻合口40~50cm处输出袢的空肠吻合。将两段肠管移近,用第3根倒刺线在浆肌层连续缝合固定空肠-空肠肠壁。缝针间距控制在0.3~0.5cm,缝合固定长度1.5~2倍于小肠径。完成小肠浆肌层缝合固定后用超声刀分别打开两侧空肠对系膜缘肠壁。用第4根倒刺线自上而下全层连续缝合两侧空肠切口后缘,完成空肠-空肠吻合口后壁的吻合。
相关知识推荐:医学sci论文难发表吗
缝合进针方向为内进内出。第4根倒刺线继续自下而上全层缝合两侧空肠切口前缘。在转向缝合空肠-空肠吻合口前壁时要调整缝线方向,由内进内出调整为外进外出,方法同前。利用第3根倒刺线自下而上浆肌层包埋空肠吻合口,并继续缝线空肠空肠吻合口后壁,完成空肠-空肠吻合口1.5圈浆肌层包埋。完成机器人下缝合后的空肠-空肠吻合口。完全机器人下全胃切除并消化道重建完毕(如图1),于耻骨上2横指处取长3~4cm切口进腹,经此口取出标本,手术结束。术后腹部切口布局如图2。
1.2.3 腹腔镜手术方法
腹腔镜手术患者采取头高脚低仰卧位(20°),两腿分开。视频车置于患者头侧。主刀医生站于患者左侧,一助站于患者右侧,扶镜手站于患者两腿之间。淋巴结清扫过程同机器人手术。完成全胃切除后,结束腹腔镜操作。于上腹正中取长12~15cm切口进腹,取出标本并检查标本。消化道重建于体外完成,食道空肠吻合口采用25cm管型吻合器完成端侧吻合,残段用60cm切割闭合器闭合。空肠-空肠吻合也采用25cm管型吻合器完成端侧吻合,60cm切割闭合器闭合残段。3-0可吸收线浆肌层包埋吻合口和小肠残段。根据需要放置腹腔引流管,清点器械、纱布无误,逐层关腹。术后部分切口分布如图3。
1.2.4 临床观察指标
主要收集手术指标、术后康复指标、标本肿瘤学指标、经济学指标及术后并发症等数据。手术指标包括:手术时间、消化道重建时间、术中出血量、切口长度。术后康复指标包括首次排气时间、首次下床活动时间、首次进食流质时间、疼痛的视觉模拟评分法(Visualanaloguescale,VAS)、术后住院时间。标本肿瘤学指标包括术后T、N、TNM分期,以及肿瘤位置、分化程度、肿瘤最长径、获取淋巴结数目、阳性淋巴结数目、上下切缘安全性、神经及脉管侵犯情况。术后并发症主要记录切口感染、吻合口瘘、吻合口出血、吻合口狭窄、术后肠梗阻、非计划30d内再次入院率等情况。经济学指标主要包括住院费用。
1.2.5 统计学方法
所有数据采用SPSS23.0软件进行统计分析。符合正态分布的计量资料以均数±标准差(x±s)表示,采用t检验进行差异分析;计数资料以相对数描述,采用χ2检验进行分析。以P<0.05为差异有统计学意义,P<0.001为差异有显著统计学意义。
2 结果
2.1两组患者手术及术后康复指标比较
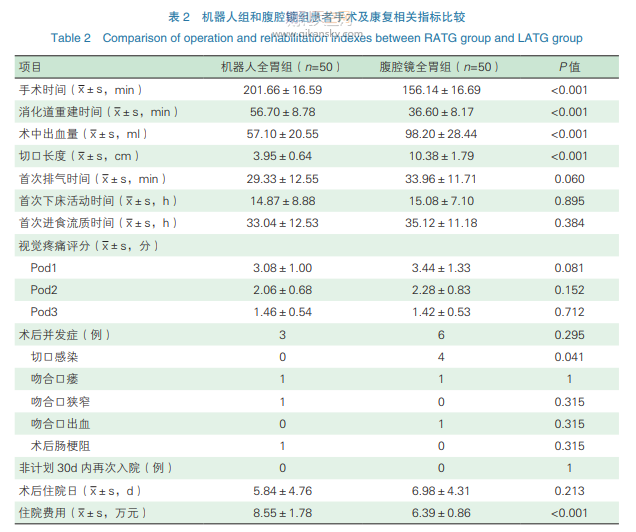
两组患者均顺利完成手术。RATG组较LATG组术中出血量少、切口短,但手术时间长、消化道重建时间长。虽然LATG组腹部切口长,但在术后3d时两组VAS疼痛评分比较,差异无统计学意义(P>0.05),这可能得益于加速康复外科多模式镇痛方案[6]。在住院费用方面,RATG组明显高于LATG组(P<0.001)。RATG组与LATG组在术后首次排气时间、首次下床活动时间、首次进食流质时间方面差异无统计学意义(P>0.05)。RATG组术后住院日短,但两组差异无统计学意义(P>0.05,见表2)。
2.2术后并发症
两组患者均未出现手术相关死亡并发症。RATG组共有3例患者出现并发症(1例吻合口瘘、1例吻合狭窄、1例术后肠梗阻);吻合口瘘患者经双套管冲洗、营养支持治疗后痊愈;术后肠梗阻患者经胃肠减压、营养支持治疗后痊愈;吻合口狭窄患者于术后45d经内镜下扩张后痊愈。LATG组共有6例患者出现术后并发症(1例吻合口瘘、1例吻合口出血、4例切口感染);吻合口瘘患者经再次手术、双套管冲洗、营养支持治疗后痊愈;吻合口出血患者经保守治疗痊愈;4例切口感染患者积极加强换药后痊愈。LATG组切口感染较多(4例),影响患者出院,导致术后住院日延长。两组患者非计划30d内再次入院率比较,差异无统计学意义(P>0.05)。
2.3肿瘤学指标
两组患者在术后T、N、TNM分期,以及肿瘤位置、分化程度、肿瘤最长径、获取淋巴结数目、阳性淋巴结数目、上下切缘安全性、神经及脉管侵犯等方面比较,差异无统计学意义(P>0.05,见表3)。
3 讨论
美国FDA批准达芬奇机器人手术系统应用于临床已有二十余年,现已在妇科、泌尿外科、心胸外科、普外科等领域得到广泛应用[7-10]。自2002年日本学者HashizumeM等[11]首次报道达芬奇机器人胃癌根治术开始,其应用于胃癌根治术的安全性不断得到验证,手术适应证不断拓宽,手术方案也在不断更新。我国学者开展达芬奇手术机器人系统胃癌根治手术已十年余,总结并发表了多篇相关研究文章。2014年余佩武团队报道了120例机器人与394例腹腔镜手术回顾性对照研究,结果显示达芬奇机器人胃癌根治术安全、可行,较腹腔镜手术有术中出血更少、淋巴结清扫更彻底、创伤更小、术后恢复更快等优势,且在3年生存率方面无差异[12]。胡建昆团队发表了关于达芬奇机器人在全胃切除脾门淋巴结清扫中应用的报道[13]。本中心江志伟教授积极探索完全机器人镜下手工缝合消化道重建技术的技巧,进一步扩大了达芬奇机器人手术系统在胃癌根治术中的优势。该方法利用达芬奇机器人手术系统结合双针四步连续缝合法完成消化道重建术,此吻合重建方法安全、有效,解决了完全机器人胃癌根治术中消化道重建的难题[14]。
完全机器人手工缝合消化道重建有以下5处关键点:①充分利用机器人第3臂:达芬奇机器人系统有4条机械臂,包括1条镜头臂和3条器械操作臂,医生只能同时控制其中的任意2条器械操作臂。所以,部分临床治疗中心认为第3臂的作用不大,可被弃用,转而依赖助手的牵拉暴露[15]。事实上,应充分利用第3臂的牵拉作用暴露术野,协助镜下缝合操作,第3臂的协同性和稳定性均比助手的抓钳效果好;②吻合缝线的选择:本团队早期的临床实践中选择普通的可吸收缝线,在连续缝合的过程中出现吻合口松散情况,收紧缝线后又出现吻合口狭窄,这会增加吻合瘘及吻合口狭窄等并发症的风险。临床实践中,本团队发现柯惠3-0倒刺线很适合吻合口缝合,该缝线质韧,对吻合口起到支撑作用,线体倒刺较多,可有效防止滑脱,降低吻合难度的同时确保了吻合口安全;③缝合方法选择:本团队采用双针四步连续缝合法,能实现吻合口的全层缝合加浆肌层包埋(双层),使吻合口安全牢靠,此缝合方法在端端、端侧和侧侧吻合中都适用;④消化道重建方案的选择:本团队在全胃切除术中采用UncutRoux-Y吻合,此方案比传统Roux-Y方案简单,避免了消化道的离断。ParisiA等[16]称这种重建方案为双环法,不仅能简化操作步骤,还能降低内疝发生率;⑤吻合口位置选择非常重要:食道空肠吻合口与Treitz韧带间肠管不宜过短,否则会压迫结肠;也不宜过长,否则会浪费肠管,建议控制在30~40cm。食道空肠吻合口距空肠空肠吻合口间的输出袢肠管距离控制在40~50cm,可起到抗返流作用。在输入袢距离食道吻合口3cm处用双股7-0丝线结扎肠管,阻断食物逆流入输入袢。在术后随访复查胃镜中发现,有1例患者出现输入袢再通,但无临床不适症状发生。
全胃切除术后完全机器人手工缝合消化道重建的优点:①进一步体现微创的优势。机器人辅助或腹腔镜辅助胃癌根治术需要取上腹部切口,该切口并不小,特别是在全胃切除的患者,通常需要长约10cm的切口才能完成食道抵钉座的安装及吻合。本团队镜下完成消化道重建后于下腹取长3~4cm切口取出标本便可,部分女性患者可以通过阴道取出标本,实现腹部无辅助切口,进一步体现了微创的优势[17]。②降低了对吻合器的依赖和手术费用。吻合器的发明降低了消化道重建的难度,但在完全腹腔镜下使用吻合器完成消化道重建难度仍较大。尽管可通过Orvil法、反穿刺法和荷包缝合法完成食道端抵钉座的放置[18],降低了完全腹腔镜下消化道重建难度,但整个操作过程还是比较复杂和困难。以进口器械为例,通常全胃切除消化道重建最少需要两把25cm管型吻合器、两枚腔镜下60cm切割闭合钉,费用在13000元以上。然而4根倒刺线费用不到3000元,一定程度上降低了患者的住院费用。③机器人镜下手工缝合简单且易掌握。杨闯等[19]报道了全胃切除术完全腹腔镜下手工缝合消化道重建,此手术对术者腔镜下缝合技术要求很高,需要腔镜下缝合熟练的外科医生完成。手术机器人具有精准、灵活、稳定的器械,在缝针的抓取、进出针角度控制和打结等方面具有明显优势,此降低了镜下缝合重建的难度,易于初学者掌握。全胃切除术后完全机器人手工缝合消化道重建的缺点:①耗时长。虽然手术机器人镜下缝合简单,但是与体外吻合器消化道重建术比较,耗时仍然比较长。为此,本团队尝试在空肠空肠吻合口采用60cm腔镜切割闭合器完成空肠空肠侧侧吻合,再于镜下用3-0倒刺线关闭共同开口并浆肌层包埋吻合口,一定程度上缩短了消化道重建时间。②住院费用高。虽然采用倒刺线完成消化道重建降低了费用,但是达芬奇机器人开机费及器械耗材费比较昂贵,此增加了患者的经济负担。期望国产机器人手术系统早日应用于临床中,并将手术机器人费用尽快纳入医保报销范围。
完全机器人手工缝合消化道重建术使达芬奇机器人手术系统在胃癌根治术中的优势得到进一步展示,希望这一方式被更多的外科医师掌握或改进,并使更多的患者获益。同时,期待有更多前瞻性随机对照研究开展,以进一步证实此全胃切除术后消化道重建方式的安全性和优势。——论文作者:刘 江1,王 刚1,冯啸波2,潘华峰1,王海锋1,江志伟1
* 稍后学术顾问联系您